Más del 40% de los medicamentos genéricos en el Perú no pasarían los estudios de bioequivalencia
En el congreso se alista la promulgación del PL del Ingreso Expedito de Medicamentos de Países de Alta Vigilancia Sanitaria, siendo una solución inmediata para incrementar la disponibilidad de estos fármacos.
- Más acceso a medicamentos seguros y eficaces: ¿Qué propone la nueva ley del Congreso?
- Medicamentos genéricos Intercambiables: El camino hacia una salud más segura y eficaz en el Perú

En el Perú, la disponibilidad de medicamentos genéricos intercambiables es alarmantemente baja. De los aproximadamente 6,000 productos farmacéuticos en el mercado, solo 113 han demostrado ser intercambiables, es decir, poseen la misma eficacia y seguridad que los medicamentos de marca. Esta situación genera incertidumbre entre los pacientes que buscan tratamientos accesibles y efectivos.
En comparación con otros países latinoamericanos como Chile, México y Brasil, donde la presencia de genéricos intercambiables es significativamente mayor, el Perú muestra un retraso notable. Esto plantea la pregunta: ¿qué sucede con el resto de los genéricos en el país?
Además del impacto en la disponibilidad de tratamientos accesibles, esta falta de medicamentos también repercute en la capacidad del sistema de salud para atender eficazmente a la población. “Con el ingreso de los medicamentos genéricos, definitivamente la que se beneficia acá es la atención primaria porque va a estar enfocada en manejar el 70 % u 80 % de las patologías”, enfatiza Omar Neyra, doctor en Salud Pública."
Una posible solución para mejorar el acceso a medicamentos genéricos intercambiables es facilitar la entrada de productos provenientes de países con alta vigilancia sanitaria. Actualmente, un proyecto de ley aprobado en primera votación busca agilizar este proceso; sin embargo, aún se espera la segunda votación programada para la primera semana de abril.
Medicamentos genéricos intercambiables y de marca: ¿Son lo mismo?
Es esencial comprender la relación entre los medicamentos genéricos intercambiables y los de marca. Pablo González, químico farmacéutico de la Universidad Católica de Chile, nos explica a través de un ejemplo gráfico con el comprimido de paracetamol de 500 MG.
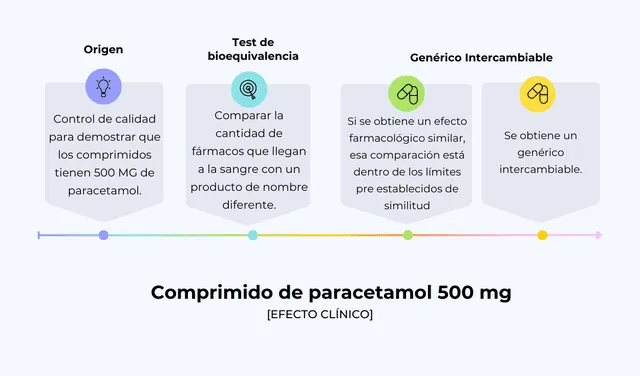
Ejemplo gráfico sobre el proceso de un medicamento. Fuente: Composición LR.
“Por tanto, el test de bioequivalencia es una comparación estandarizada en la concentración plasmática o sanguíneas en un producto que quiere demostrar bioequivalencia en comparación con un producto que la entidad regulatoria ha definido como referente. Entonces, si esa comparación está dentro de límites preestablecidos de similitud, y se tiene evidencia experimental, es un genérico intercambiable”, recalca.
¿Por qué tomar conciencia sobre la importancia de la ley de medicamentos genéricos?
Garantizar la disponibilidad de medicamentos bioequivalentes en el mercado peruano es crucial para asegurar tratamientos de calidad, seguros y eficaces. Estos medicamentos permiten que más personas accedan a terapias sin enfrentar barreras económicas o de disponibilidad. Además, los genéricos intercambiables han demostrado tener un impacto positivo en la reducción del gasto gubernamental en salud, como se ha observado en países como Chile.
“Para el caso de Chile, no solo se aumentó el acceso, sino que también tuvo un impacto positivo en el gasto gubernamental en medicamentos porque el Gobierno tiene programas donde asegura a la población la terapia medicamentosa para ciertas patologías. Por lo tanto, la existencia de bioequivalentes en el mercado, le permitió disminuir el gasto público en medicamentos, pero sin sacrificar calidad, seguridad y eficacia”, indica Pablo González.
Así pues, el hecho de contar con medicamentos genéricos ya sea para enfermedades crónicas u otro tipo de patologías, “rápidamente mejora todo el sistema de atención primaria y la salud pública en general”, resalta Omar Neyra, doctor en Salud Pública.
Políticas de intercambiabilidad en otros países Latinoamericanos
En Chile, la Política Nacional de Medicamentos comenzó en 2004, estableciendo un marco legal para la bioequivalencia, prueba universal para demostrar la intercambiabilidad de medicamentos. Seis años después, un decreto supremo amplió la aplicación de la bioequivalencia a nivel nacional.
“En el año 2012 comienza la bioequivalencia en Chile, dando pequeños pasos, escogiendo pequeños productos que fueran ejemplos de bioequivalencia in vitro que fue la clorfenamina y estudio de bioequivalencia en vivo cómo fue la carbamazepina”, explica el químico farmacéutico Pablo González.
En 2013, el Instituto de Salud Pública (ISP)—equivalente a DIGEMID en Perú—estableció cronogramas para evaluar principios activos en ciertas formas farmacéuticas.
“Estos cronogramas se fueron emitiendo cada cierto tiempo, y en estos se establecía un plazo para que, desde la fecha de publicación del cronograma, los fabricantes presentarán los resultados del estudio. Los plazos fueron entre 18 a 24 meses, de esa forma se operativizó el avance de la bioequivalencia en Chile, por parte de la ISP”, añade González.

La disponibilidad de medicamentos seguros y accesibles mejora la salud pública.
A pesar del tiempo transcurrido, Perú no ha seguido el mismo modelo. Factores como la falta de información y obstáculos regulatorios han limitado la disponibilidad de medicamentos genéricos intercambiables. “Hoy no tenemos medicamentos de calidad a bajo costo, especialmente para una población peruana que es la que más necesita”, advierte Omar Neyra, doctor en Salud Pública.
Situación actual del ingreso de los medicamentos genéricos
Desde la implementación de la norma de bioequivalencia en Chile, han pasado 13 años, con avances progresivos en la comunicación y acceso a medicamentos.
“En Chile, se decidió que a los medicamentos que contaban con bioequivalencia se los iba a identificar con un logo amarillo y dentro de ello iba la palabra “bioequivalente” en letras rojas. Esto se convirtió en el slogan de una campaña del Ministerio de Salud, conocida como “Exige el amarillo”, señala el químico farmacéutico.
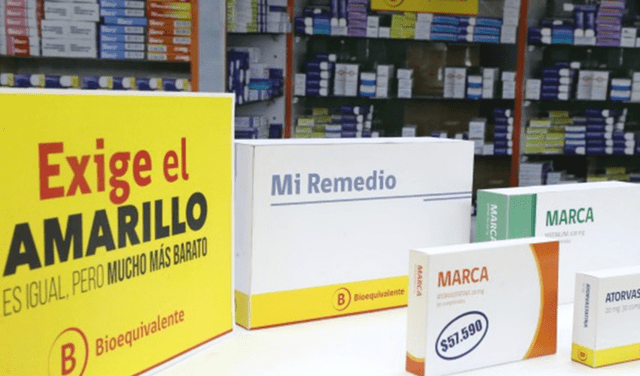
Difusión de los medicamentos genéricos intercambiables en Chile. Fuente: Difusión.
En contraste, en Perú, la falta de acceso a la información y estrategias de difusión impide que los pacientes conozcan sus derechos y opciones de tratamiento.
“Lo que toca ahora es informar a la población, a través de todas las vías posibles. Pero también nos toca un gran trabajo en los procesos regulatorios y en las normas conexas que implica la implementación de la ley porque solo con la ley no va a empezar a funcionar todo esto”, finaliza el viceministro de Salud Pública Eric Peña.
La limitada disponibilidad de medicamentos genéricos intercambiables en el Perú subraya la urgencia de implementar políticas que faciliten su acceso y promuevan su uso. Aprender de experiencias exitosas en otros países y agilizar los procesos regulatorios son pasos esenciales para garantizar que más peruanos puedan beneficiarse de tratamientos seguros, eficaces y asequibles.
[CONTENIDO PATROCINADO]